疫苗是预防传染病最有效的方法之一,天花、脊髓灰质炎等都是靠疫苗才得以消灭。近年来,我国疫苗行业发展迅速,年批签发量超过6亿支,市场规模达到350亿元。新冠肺炎疫情下,我国疫苗行业进入了一个新的发展阶段,在与疫情赛跑的过程中,新冠疫苗研发生产的经验也给我国疫苗行业带来了新的发展机遇。
中国复星/德国BioNTech的新冠疫苗在中国香港紧急获批,也成为第一款在大中华区域获批上市mRNA疫苗。
中国国家药品监督管理局药品审评中心官网最新公示PG电子网址,由赛诺菲巴斯德和阿斯利康联合开发的预防呼吸道合胞病毒感染的长效单克隆抗体nirsevimab正式获准纳入突破性治疗药物程序。
埃及正式批准在埃紧急使用中国国药集团新冠灭活疫苗,中国新冠疫苗的安全性和有效性已得到科学认证。
印尼,从中国科兴公司订购的300万剂疫苗已抵达,目前正向全国分发,未来还有1.225亿剂科兴疫苗陆续抵达。
秘鲁已与中国国药集团达成购买该集团生产的新冠灭活疫苗协议,首批100万剂疫苗将于本月抵达秘鲁。

康希诺生物宣布新冠疫苗3期试验获积极结果,成功达到预设的主要安全性及有效性标准,未发生任何与疫苗相关的严重不良事件(SAE)。
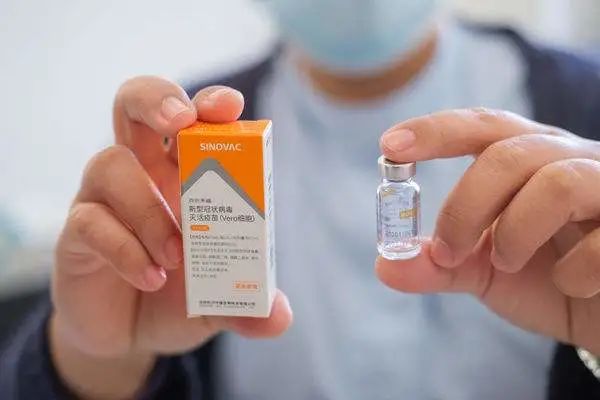
国家药监局附条件批准科兴中维新冠疫苗上市注册申请,国家药监局要求该疫苗上市许可持有人继续开展相关研究工作,完成附条件的要求PG电子平台,及时提交后续研究结果。
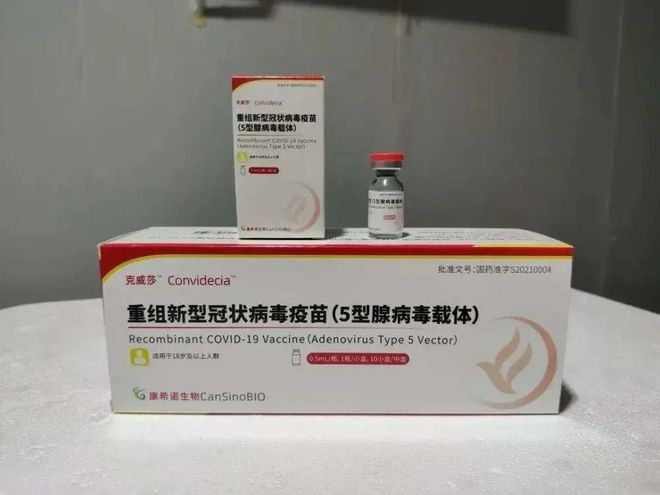
由中国工程院院士、军事科学院军事医学研究院研究员陈薇领衔的团队研发的我国重组新冠病毒疫苗(腺病毒载体),获国家药品监督管理局附条件批准上市注册申请。是我国首家获批的腺病毒载体新冠病毒疫苗。
科兴生物发布全球首个未成年人组新冠疫苗临床研究数据中不仅安全性良好,免疫原性也良好,且明显优于和老人。
我国重组蛋白新冠病毒疫苗I期II期临床试验结果发布:接种3剂次疫苗后,97%的人可以产生中和抗体。
国药集团中国生物新冠疫苗大规模紧急使用安全性数据发布,一般反应的发生率较低,未见严重不良反应,疫苗具有良好的安全性。
国药集团中国生物研究院重组新冠病毒疫苗获得国家药品监督管理局临床试验批件。这是继国药集团中国生物两款新冠灭活疫苗后,又一技术路线的新冠疫苗获批临床,成为中国生物第三款新冠疫苗。
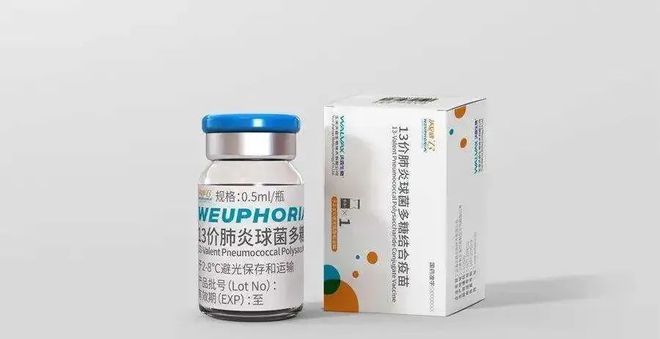
康希诺生物股份公司研发的13价肺炎球菌多糖结合疫苗(CRM197,TT载体),已完成Ⅲ期临床试验准备工作,正式进入Ⅲ期临床试验。
国家疾病预防控制局正式挂牌,标志着疾控机构职能从单纯预防控制疾病向全面维护和促进全人群健康转变。
东方高圣重磅发布了国内第一本针对疫苗产业调研的——《中国疫苗》(以下简称“《》”)。与此同时,以“疫苗投行”为业务定位的东方高圣苏州公司正式成立开业。
沃森生物启动四价疫苗国际临床试验,实现了沃森海外临床零的突破,并参与联合国儿童基金会COVAX投标。
科兴研制的新冠病毒灭活疫苗克尔来福®通过了世界卫生组织(WHO)评审,正式列入世界卫生组织紧急使用清单。
科兴EV71疫苗益尔来福获批扩龄使用,接种对象适用年龄范围由原来的6月龄至3岁扩大为6月龄至71月龄。
中国医学科学院医学生物学研究所自主研发的科维福新型冠状病毒灭活疫苗首批上市,供国内紧急使用,全程接种两剂。
韩国SK生物科学(SK Bioscience)决定将斥资1500亿韩元(约合人民币8.5亿元)扩建旗下位于庆尚北道安东市的疫苗生产厂。
全球疫苗免疫联盟宣布,已同中国国药集团和科兴公司签署大批量预购协议,这意味着国药疫苗和科兴疫苗进入“新冠肺炎疫苗实施计划”(COVAX)疫苗库。
国家药监局药品监管司司长袁林在国务院政策例行吹风会上介绍,国家药监局已经应急批准了5条技术路线个疫苗品种进入临床试验,依法依规附条件批准了4个新冠病毒疫苗上市。
赛诺菲巴斯德宣布每年将投资约4亿欧元,推动首个mRNA疫苗卓越中心的建设。该中心将致力于加速下一代疫苗的开发与供应。到2025年,该mRNA疫苗卓越中心预计将研发出至少6 款临床候选疫苗。
Moderna公司:基于mRNA技术品台的艾滋病病毒(HIV)疫苗的临床试验,并计划于2023年春季完成。
服贸会上,国药集团中国生物研发的新一代新冠疫苗亮相,不仅有针对变异毒株的灭活疫苗,还有广谱的重组蛋白疫苗,自主研发的mRNA疫苗。
从中国疾控中心获悉,我国已完成针对德尔塔变异株灭活疫苗的临床前研究。各疫苗研发单位还开展了针对贝塔株、德尔塔株的腺病毒载体疫苗和核酸疫苗研发工作。
美国斯坦福大学和北卡罗莱纳大学教堂山分校的研究人员创造了一种3D打印疫苗贴片,无需注射,效果比传统注射强十倍。
康泰生物发布公告,称其子公司民海生物13价肺炎球菌多糖结合疫苗上市申请获得药监局的批准,用于2月龄-5 周岁婴幼儿和儿童。这是全球第3家获得13价肺炎球菌多糖结合疫苗药品注册证书的企业。

艾博生物,通过江苏省药品监督管理局的药品生产许可证核发审查,获得江苏省首张mRNA疫苗生产许可证,生产范围为预防用生物制品(新型冠状病毒mRNA疫苗)。
 PG电子·(中国)官方网站
PG电子·(中国)官方网站